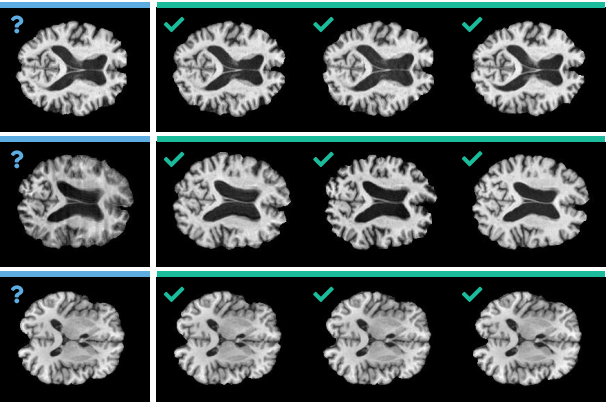
DeepBrainPrint è un framework di deep learning contrastivo per la ri-identificazione di soggetti tramite MRI cerebrali, accettato alla conferenza Medical Imaging with Deep Learning (MIDL) 2023. Nel panorama del brain fingerprinting, DeepBrainPrint rappresenta il primo approccio semi-auto-supervisionato, capace di estrarre una “impronta numerica” dalla morfologia cerebrale che consente il recupero efficace di tutte le scansioni relative allo stesso soggetto da grandi dataset di imaging medico.
Motivazioni & Obiettivi
- Consentire la ri-identificazione automatica di pazienti (brain re-identification) all’interno di database di MRI sempre più estesi, semplificando la gestione longitudinale delle acquisizioni cliniche.
- Migliorare la robustezza dell’identificazione, superando le limitazioni dei metodi precedenti in presenza di variazioni dovute ad invecchiamento, progressione di malattia, differenze di scanner e sequenza di acquisizione.
- Gettare le basi per nuovi sistemi di retrieval morfologico, utili anche per la ricerca di pazienti simili in ambito clinico e ricerca comparativa.
- Pipeline contrastiva semi-auto-supervisionata, che combina apprendimento self-supervisionato e supervisione debole per creare rappresentazioni numeriche (fingerprint) robuste della morfologia cerebrale.
- Innovazioni principali:
- Funzione di loss adattiva per guidare meglio la convergenza del modello.
- Nuove trasformazioni di immagine per aumentare la robustezza rispetto a differenze di intensità (contrasti), aging e patologia.
- Test estesi su T1-weighted MRI (ADNI) e dataset sintetici multimodali.
- DeepBrainPrint supera tecniche di deep metric learning all’avanguardia (InfoNCE, SoftTriple, SimCLR, BarlowTwins) sia in accuratezza, sia in efficienza computazionale e capacità di generalizzazione su soggetti diversi.
- Il modello si presta oltre alla ri-identificazione anche alla ricerca automatica di scansioni con caratteristiche morfologiche simili (ad es. per shape, lesioni, atrofie), utile anche tra pazienti diversi.
- Soluzione scalabile, pronta per essere adottata in grandi biobanche e reti sanitarie.
Articoli Scientifici Correlati
- DeepBrainPrint: A Novel Contrastive Framework for Brain MRI Re-Identification arXiv preprint arXiv:2302.13057 (2023) – MIDL Proceedings Autori: Lemuel Puglisi, Frederik Barkhof, Daniel C. Alexander, Geoffrey JM Parker, Arman Eshaghi, Daniele Ravì
Team & Autori
- Lemuel Puglisi (Primo autore, sviluppo metodologico)
- Daniele Ravì (Coautore, supervisione scientifica)
- Frederik Barkhof, Daniel C. Alexander, Geoffrey JM Parker, Arman Eshaghi (Coautori, supervisione, supporto dati)